На первый взгляд кажется, что вопрос о количестве молекул кислорода в 8 г – это очень сложный вопрос, который требует глубоких знаний в области химии и молекулярной физики. Однако, существует простая формула, которая позволяет найти это количество: массу одной молекулы кислорода, атом которого обозначается символом O, можно определить с помощью молярной массы.
Молярная масса – это масса одного моля вещества, выраженная в граммах. Для кислорода молярная масса равна приблизительно 32 г/моль. Теперь, чтобы найти массу одной молекулы кислорода нужно разделить молярную массу на числовую постоянную Авогадро. Числовая постоянная Авогадро равна приблизительно 6,02214076×10^23 молекул/моль.
Итак, чтобы найти количество молекул кислорода в 8 г, необходимо разделить массу на массу одной молекулы. Подставим значения: 8 г / (32 г/моль) * (6,02214076×10^23 молекул/моль). После простых математических вычислений получаем ответ: в 8 г кислорода содержится примерно 1,50553519×10^23 молекул.
Сколько молекул содержится в 8 г кислорода?

Для расчета количества молекул необходимо знать молярную массу кислорода. Молярная масса кислорода равна 32 г/моль.
Сначала найдем количество молей кислорода, используя формулу:
моли = масса / молярная масса
Подставив известные значения, получим:
моли = 8 г / 32 г/моль = 0,25 моль
Далее необходимо умножить количество молей на постоянную Авогадро (6,022 x 10^23 молекул/моль), чтобы найти количество молекул:
количество молекул = количество молей x постоянная Авогадро
Подставив известные значения, получим:
количество молекул = 0,25 моль x 6,022 x 10^23 молекул/моль = 1,5055 x 10^23 молекул
Таким образом, в 8 г кислорода содержится приблизительно 1,5055 x 10^23 молекул.
Формула расчета количества молекул кислорода

Для расчета количества молекул кислорода в заданной массе необходимо использовать следующую формулу:
1. Вычислите молярную массу кислорода (O). Величина молярной массы кислорода равна приблизительно 16 г/моль (точное значение составляет 15,999 г/моль).
2. Примените формулу:
- Масса (в г) / Молярная масса (в г/моль) = Мольные единицы кислорода (в моль)
- Мольные единицы кислорода (в моль) * 6,022 × 10^23 = Количество молекул кислорода
Например, если у нас есть 8 г кислорода:
- 8 г / 16 г/моль = 0,5 моль кислорода
- 0,5 моль * 6,022 × 10^23 = 3,011 × 10^23 молекул кислорода
Таким образом, в 8 г кислорода содержится приблизительно 3,011 × 10^23 молекул кислорода.
Молярная масса кислорода
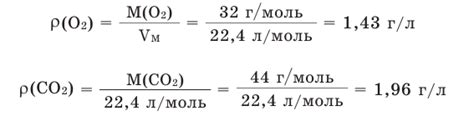
Масса одного атома кислорода составляет примерно 16 атомных единиц (у), а количество атомов в одном моле равно постоянной Авогадро и составляет примерно 6.022 x 10^23 атомов.
Поэтому, чтобы найти молярную массу кислорода, нужно умножить массу одного атома на количество атомов в одном моле:
- Масса одного атома кислорода: 16 у;
- Количество атомов в одном моле: 6.022 x 10^23 атомов.
Теперь, чтобы рассчитать молярную массу кислорода, нужно умножить массу одного атома на количество атомов:
Молярная масса кислорода = 16 у x 6.022 x 10^23 атомов/моль.
Таким образом, молярная масса кислорода равна примерно 96 г/моль.
Теперь, зная молярную массу кислорода, можно рассчитать количество молекул в заданной массе кислорода. Для этого нужно разделить массу кислорода на его молярную массу и умножить результат на постоянную Авогадро:
Количество молекул = масса кислорода / молярная масса кислорода x постоянная Авогадро.
Например, для 8 г кислорода:
Количество молекул = 8 г / 96 г/моль x 6.022 x 10^23 атомов/моль.
Таким образом, в 8 г кислорода содержится примерно 5.01 x 10^23 молекул.
Количество молей в 8 г кислорода

Для определения количества молекул в 8 г кислорода необходимо сначала вычислить количество молей данного вещества. Для этого воспользуемся формулой:
| Масса вещества (г) | Молярная масса (г/моль) | Количество молей |
| 8 г | 32 г/моль | 0.25 моль |
Молярная масса кислорода равна 32 г/моль. Для определения количества молей в 8 г кислорода, мы делим массу кислорода на его молярную массу:
8 г / 32 г/моль = 0.25 моль
Таким образом, в 8 г кислорода содержится 0.25 моль. Чтобы определить количество молекул, необходимо умножить количество молей на постоянную Авогадро (6.02214076 × 10^23 молекул/моль):
0.25 моль * 6.02214076 × 10^23 молекул/моль = 1.50553519 × 10^23 молекул
Таким образом, в 8 г кислорода содержится приблизительно 1.50553519 × 10^23 молекул.
Количество атомов в одной молекуле кислорода
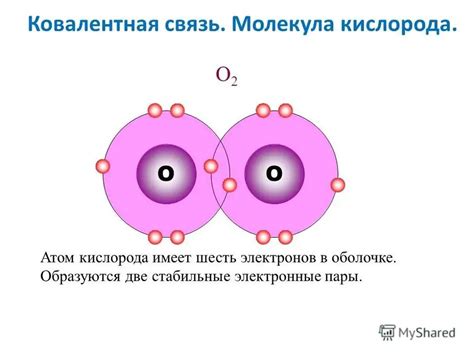
Молекула кислорода (O2) состоит из двух атомов кислорода, связанных между собой. Таким образом, в одной молекуле кислорода содержится 2 атома.
Количество молекул кислорода в 8 г
Для расчета количества молекул кислорода в 8 г необходимо использовать формулу расчета количества молей вещества и формулу Авогадро.
Молярная масса кислорода (O2) равна 32 г/моль, так как атом кислорода имеет атомный вес 16. Таким образом, 1 моль кислорода содержит 6,023 х 1023 молекул по формуле Авогадро.
Для расчета количества молекул кислорода в 8 г нужно найти количество молей кислорода в данном образце.
| Масса кислорода, г | Молярная масса кислорода, г/моль | Количество молей кислорода | Количество молекул кислорода |
|---|---|---|---|
| 8 | 32 | 0,25 | 1,51 х 1023 |
Таким образом, в 8 г кислорода содержится приблизительно 1,51 х 1023 молекул кислорода.
Способы подсчета количества молекул кислорода

1. Использование молярной массы
Для подсчета количества молекул кислорода можно воспользоваться молярной массой данного вещества. Молярная масса кислорода равна примерно 16 г/моль.
Если известна масса кислорода, необходимо разделить ее на молярную массу, чтобы получить количество молей. Затем количество молей умножается на постоянную Авогадро (около 6,02 * 10^23 молекул/моль), чтобы определить количество молекул кислорода.
Например, если имеется 8 г кислорода:
Количество молей кислорода = масса кислорода / молярная масса кислорода = 8 г / 16 г/моль = 0,5 моль
Количество молекул кислорода = количество молей кислорода * постоянная Авогадро = 0,5 моль * 6,02 * 10^23 молекул/моль = 3,01 * 10^23 молекул
2. Использование количества вещества
Также можно использовать количества вещества для подсчета количества молекул кислорода. Количество вещества измеряется в молях и определяется через соотношение между массой вещества и его молярной массой.
Если имеется молей кислорода, количество молекул можно определить, умножив количество молей на постоянную Авогадро.
3. Количественный состав вещества
Еще одним способом подсчета количества молекул кислорода является использование количественного состава вещества. Например, если известно, что водный раствор кислорода содержит 89% кислорода, можно использовать эту информацию для рассчета количества молекул.
Для этого необходимо умножить процентное содержание кислорода на общее количество молекул вещества.
Например, если имеется 100 молекул вещества:
Количество молекул кислорода = процентное содержание кислорода * общее количество молекул = 89% * 100 молекул = 89 молекул
Важно помнить, что эти способы подсчета молекул кислорода являются приближенными и не учитывают все факторы, такие как примеси и условия эксперимента. Однако, они дадут достаточно точные результаты для большинства практических задач.
Значение данного расчета в химии

Данная формула позволяет определить количество молекул кислорода в данном количестве вещества, выраженном в граммах. Такой расчет основан на молярной массе кислорода и числе Авогадро.
Знание количества молекул вещества позволяет определить их концентрацию, проводить реакции на молекулярном уровне, сравнивать вещества между собой по количеству частиц и прогнозировать результаты реакций.
Этот расчет также позволяет определить стехиометрические соотношения между различными реагентами, что позволяет планировать эксперименты, проводить анализ реакций и оптимизировать процессы получения химических продуктов.
Важно отметить, что такие расчеты основаны на идеальных условиях и предполагают, что реакция протекает без потерь и в полном соответствии с законами химии. Однако в реальной жизни могут возникать неконтролируемые факторы, которые могут повлиять на результаты расчетов.
Таким образом, значение данного расчета в химии заключается в его применимости для определения количества молекул вещества, которое является фундаментальным показателем в химических исследованиях и позволяет установить связь между массой вещества и количеством молекул.
Другие примеры расчета количества молекул
Расчет количества молекул вещества может быть использован в различных химических и физических задачах. Например, для определения массы определенного количества вещества, необходимого для реакции, или для оценки концентрации вещества в растворе.
Рассмотрим несколько примеров расчета количества молекул вещества:
Пример 1:
Сколько молекул содержится в 12 г воды (H2O)?
Для решения данной задачи необходимо знать молярную массу воды. Молярная масса воды равна 18 г/моль (2 г за каждый атом водорода и 16 г за атом кислорода).
Далее, используя формулу расчета количества молекул, можно получить следующий результат:
N = m/M
где N - количество молекул, m - масса вещества, M - молярная масса вещества.
В нашем примере:
N = 12 г / 18 г/моль = 0.67 моль
Таким образом, в 12 г воды содержится примерно 0.67 моль молекул воды.
Пример 2:
Сколько молекул содержится в 5 г глюкозы (C6H12O6)?
Молярная масса глюкозы равна 180 г/моль (12 г за каждый атом углерода, 1 г за каждый атом водорода и 16 г за атом кислорода).
Применяя формулу расчета количества молекул, получим следующий результат:
N = m/M
где N - количество молекул, m - масса вещества, M - молярная масса вещества.
В нашем примере:
N = 5 г / 180 г/моль = 0.028 моль
Следовательно, в 5 г глюкозы содержится примерно 0.028 моль молекул глюкозы.
Использование данной формулы для других веществ
Формула расчета количества молекул вещества может быть использована не только для кислорода, но и для других химических элементов или соединений. Для этого необходимо знать молярную массу данного вещества.
Молярная масса - это масса одного моля (6.022 × 10^23 частиц) вещества. Она выражается в г/моль. Чтобы использовать формулу расчета количества молекул, необходимо знать молярную массу вещества и массу данного вещества в граммах.
Формула расчета:
Количество молекул = (масса вещества в г) / (молярная масса вещества в г/моль) × (6.022 × 10^23 молекул/моль)
Например, если нам необходимо рассчитать количество молекул в 10 г углекислого газа (CO2), то необходимо знать молярную массу CO2, которая равна около 44 г/моль.
Количество молекул CO2 = (10 г) / (44 г/моль) × (6.022 × 10^23 молекул/моль) ≈ 1.37 × 10^23 молекул
Таким же образом можно рассчитать количество молекул для любого химического элемента или соединения, если известна его молярная масса и масса вещества в граммах.
Важно помнить, что формула расчета количества молекул применима только для химических веществ, где межатомные связи представляют собой ковалентные связи. Для ионных веществ применяется другая формула.
Применение полученной информации в практических задачах и исследованиях

Полученная информация о количестве молекул в 8 г кислорода может быть полезна в различных практических задачах и исследованиях, связанных с химическими реакциями и расчетами.
Например, зная количество молекул в заданном количестве вещества, можно производить расчеты массы других веществ, участвующих в реакции. Для этого необходимо знать коэффициенты взаимодействия веществ в химическом уравнении.
Также, эта информация может быть полезна при проведении экспериментов, где требуется точно определить количество вещества, например, при синтезе нового вещества или при подготовке растворов с определенной концентрацией.
Другим применением этой информации является расчет стехиометрического коэффициента в реакциях. Стэхиометрические коэффициенты позволяют определить пропорцию между количеством реагентов и продуктов реакции.
Кроме того, данная информация может быть использована для моделирования химических реакций на компьютере или в химических программных пакетах, которые позволяют проводить расчеты и проводить виртуальные эксперименты.
| Возможное применение | Примеры инженерных задач и исследований |
|---|---|
| Синтез новых веществ | Разработка новых материалов с определенными свойствами |
| Расчет концентрации раствора | Определение необходимого количества реагентов для получения раствора заданной концентрации |
| Определение массы продукта реакции | Расчет количества продукта реакции или потребляемых реагентов |
| Моделирование химических реакций | Исследование влияния различных факторов на ход химической реакции |
Все эти примеры демонстрируют, что получение и использование информации о количестве молекул вещества позволяет проводить различные практические задачи и исследования в области химии.



