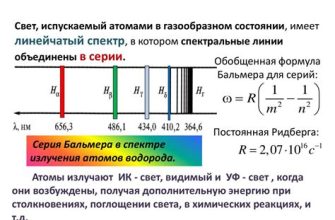
Внешняя электронная оболочка иона Ca2+ состоит из двух электронов. Они заполняют электронные уровни 3s и 3p, образуя замкнутую сферическую область вокруг ядра иона кальция.
Аналогичное строение внешнего слоя имеет ион Mg2+, который является ионом магния с двумя отданными электронами. Они также заполняют электронные уровни 3s и 3p, образуя ту же замкнутую сферическую область вокруг ядра иона магния, что и ион кальция.
Это строение внешнего слоя позволяет иону кальция и иону магния образовывать стабильные соединения и принимать участие в химических реакциях. Кроме того, ион Ca2+ и ион Mg2+ имеют похожую валентность, что также обуславливает их схожее строение внешнего слоя.
Ион Ca2+

Ион Ca2+ является ионом кальция с положительным зарядом. Он образуется, когда атом кальция теряет два электрона из своего внешнего энергетического слоя, состоящего из двух электронов. Потеря электронов приводит к образованию положительного заряда, так как заряд протонов в атоме остается неизменным, а количество электронов уменьшается.
Внешний слой иона Ca2+ имеет аналогичное строение, как и внешний слой атома газа Хе. Оба слоя состоят из двух электронов, что делает ион Ca2+ по своим свойствам ионом инертного газа. Ион Ca2+ проявляет свойства инертных газов взаимодействуя с другими элементами и соединениями.
Таблица позволяет сравнить строение внешних слоев атомов и ионов Ca2+ и Хе:
| Атом или ион | Внешний энергетический слой |
|---|---|
| Ca | [2] |
| Ca2+ | [2] |
| Хе | [2] |
Как видно из таблицы, внешний слой атомов и ионов Ca2+ и Хе состоит из двух электронов, что объясняет их сходство в строении внешнего слоя.
Внешний слой
Внешний слой атома или иона представляет собой последнюю энергетическую оболочку, на которой располагаются электроны. Этот слой играет важную роль в химических реакциях и взаимодействии атомов между собой.
Атомы ионы могут иметь различное количество электронов в своем внешнем слое. У иона Ca2+ внешний слой состоит из двух электронов.
Атомы, имеющие аналогичное строение внешнего слоя, проявляют сходные химические свойства. Поэтому атомы с одинаковым числом электронов во внешнем слое образуют группы элементов в периодической системе. Например, к группе, в которую входит ион Ca2+, относятся другие элементы, такие как Sr2+ и Ba2+, у которых также два электрона во внешнем слое.
Знание строения внешнего слоя атомов и ионов помогает понять их реакционную способность и возможность образования химических связей.
Строение внешнего слоя
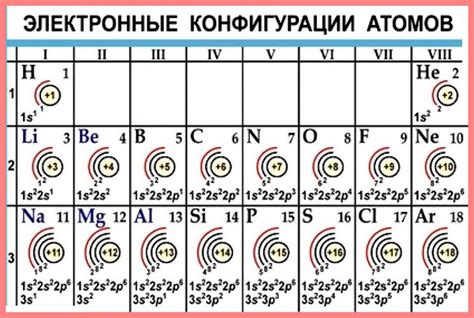
Внешний слой атома, также известный как валентная оболочка, определяет его химические свойства и взаимодействие с другими атомами. Валентная оболочка состоит из электронных оболочек, каждая из которых содержит определенное количество электронов.
Атом кальция (Ca) имеет 20 электронов. Его внешний слой состоит из двух электронных оболочек: s-оболочки с 2 электронами и p-оболочки с 6 электронами. Это означает, что внешний слой кальция содержит 8 валентных электронов.
Атомы, у которых количество валентных электронов соответствует иону Ca2+, имеют аналогичное строение внешнего слоя. Такие атомы могут находиться в той же группе периодической системы элементов, что и кальций.
Например, элементы группы 2 (группы щелочноземельных металлов) периодической системы элементов, такие как магний (Mg), стронций (Sr) и барий (Ba), имеют аналогичное строение внешнего слоя и также содержат по 8 валентных электронов.
Строение внешнего слоя атомов очень важно при реакциях и химических связях между атомами. Атомы обычно стремятся заполнить свой внешний слой, чтобы достичь стабильной конфигурации электронов.
| Элемент | Количество валентных электронов |
|---|---|
| Магний (Mg) | 8 |
| Кальций (Ca) | 8 |
| Стронций (Sr) | 8 |
| Барий (Ba) | 8 |
Аналогичное строение внешнего слоя
Аналогичное строение внешнего электронного слоя, как и ион Ca2+ (ион кальция), имеют атомы других щелочноземельных металлов из группы 2 периодической системы Менделеева.
Эти атомы также обладают двумя электронами в своем внешнем энергетическом уровне, что делает их аналогичными иону Ca2+ с точки зрения химических свойств и взаимодействий.
Список атомов с аналогичным строением внешнего слоя:
- Магний (Mg)
- Бериллий (Be)
- Стронций (Sr)
- Барий (Ba)
- Радий (Ra)
Эти атомы образуют ионы со зарядом +2, потому что, чтобы достичь наиболее стабильной электронной конфигурации, им необходимо отдать два электрона из внешнего энергетического уровня. Также, в соединениях они обычно вступают в реакции, подобные реакциям иона Ca2+.
Таким образом, ионы магния, бериллия, стронция, бария и радия являются химически аналогичными иону кальция и имеют сходные свойства и взаимодействия.
Атом с аналогичным строением
Атом, имеющий аналогичное строение внешнего слоя, как и ион Ca2+, является атомом магния (Mg).
Как и ион кальция, атом магния также находится во второй группе периодической системы элементов и имеет два электрона на внешнем энергетическом уровне. Это делает ион магния и ион кальция схожими по химическим свойствам.
Также, структурная формула ионов Ca2+ и Mg2+ схожа, они оба имеют +2 заряд и несут два положительных элементарных заряда.
Однако, несмотря на аналогичное строение внешнего энергетического уровня, у магния присутствует атомный радиус и ионный радиус меньше, чем у кальция. Это объясняется большей эффективностью экранировки заряда ядра в атоме ионом магния.
Из часто встречающихся соединений, содержащих ион магния, можно назвать хлорид магния (MgCl2), оксид магния (MgO) и сернокислый магний (MgSO4).
Сходство ионов Ca2+ и Na+
Ион Ca2+ и ион Na+ имеют сходное строение внешнего слоя электронов. Оба иона имеют два электрона на валентной оболочке.
Однако, есть некоторые отличия в расположении электронов на внешней оболочке. У иона Ca2+ на внешней оболочке находятся 2 электрона в s-орбитали, в то время как у иона Na+ на внешней оболочке находится 1 электрон в s-орбитали.
Именно это отличие в валентной оболочке делает ионы Ca2+ и Na+ различными по свойствам. Ион Ca2+ имеет большую положительную заряду и образует более крепкие ионо-ковалентные связи с другими атомами.
Это объясняет, почему ион Ca2+ играет важную роль в обеспечении прочности костей и зубов, а также в регуляции множества биохимических процессов в организме.
Ион Na+, напротив, образует более слабые ионо-ковалентные связи и обладает меньшей положительной зарядой, что позволяет ему выполнять различные функции в организме, такие как передача нервных импульсов и поддержание водно-солевого баланса.
Полезность сходства
Аналогичное строение внешнего слоя как у иона Ca2+ имеет атом вещества, состоящего из этого иона - атом кальция (Ca). Это сходство внешних слоев делает их химические свойства схожими.
Сходство внешнего электронного слоя Ca2+ и атома кальция (Ca) обусловлено тем, что ион Ca2+ образуется при потере двух электронов атомом кальция (Ca). При этом оба имеют одинаковую электронную конфигурацию - 2,8,8,2. Это означает, что оба атома имеют 2 электрона в первом энергетическом уровне (K-оболочке), 8 электронов во втором (L-оболочке) и 8 электронов в третьем (M-оболочке) и дополнительно 2 электрона в своем внешнем слое.
Из-за этого сходства внешнего электронного слоя, атом кальция (Ca) и ион Ca2+ имеют схожую реакционную способность. Они обладают подобными свойствами, такими как способность образовывать ионы, вступать в химические реакции и образовывать неорганические соединения. К примеру, ион Ca2+ и атом кальция (Ca) могут образовывать соединения с антиобразующими и отрицательными ионами, такими как антиобразующи ионы и оксиды, и создавать с ними стабильные соединения.
Вопрос-ответ
Какой атом имеет аналогичное строение внешнего слоя, как и ион Ca2+?
Аналогичное строение внешнего слоя, как и ион Ca2+, имеет ион другого алкалиноземельного металла - Mg2+ (магний), т.к. ион Ca2+ и ион Mg2+ оба имеют два валентных электрона в своем внешнем электронном слое.
Что такое алкалиноземельные металлы?
Алкалиноземельные металлы - это элементы, которые находятся во второй группе периодической таблицы, сразу после алкалийных металлов. Они включают бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Все эти элементы имеют два валентных электрона в своем внешнем электронном слое.
Почему ион Ca2+ имеет аналогичное строение внешнего слоя с другими элементами во второй группе периодической таблицы?
Ион Ca2+ имеет аналогичное строение внешнего слоя с другими элементами во второй группе периодической таблицы, так как он имеет два отдельных валентных электрона в своем внешнем электронном слое. Это делает его электронную конфигурацию стабильной, что является наиболее выгодным состоянием для атома.
Какой атом взаимодействует с ионом Ca2+ в химических реакциях?
Ион Ca2+ взаимодействует с различными атомами в химических реакциях в зависимости от условий и окружающей среды. Например, в водных растворах ион Ca2+ может образовывать связи с отрицательно заряженными атомами кислорода в молекулах воды или осаждаться на поверхности других материалов, таких как кости и зубы.
Какая роль иона Ca2+ в организме?
Ион Ca2+ играет важную роль в организме. Он участвует в многих биологических процессах, включая сокращение мышц, передачу нервных импульсов, секрецию гормонов и коагуляцию крови. Также кальций является важным компонентом костей и зубов, обеспечивая им прочность и стабильность.